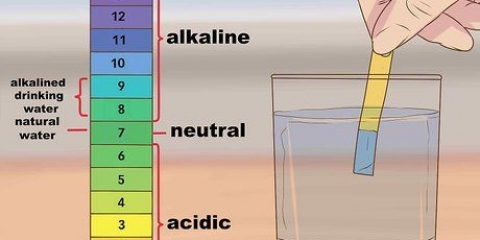
Natriumklorid (eller bordssalt) är en elektrolyt som hjälper till att förbättra vattnets ledningsförmåga. Vatten i sig är inte en särskilt bra ledare. Genom att förbättra vattnets ledningsförmåga flyter elektriciteten från batteriet lättare genom det, så att vattnet bättre delas upp i väte och syre. 
Grafitledningarna i pennorna fungerar som elektroder och leder den elektricitet som kommer från batteriet. Grafit är mycket lämpligt eftersom det inte kommer att lösas upp eller skadas av vattnet under experimentet. 
Kartongbiten låter dig låta pennornas grafitledningar hänga i vattnet utan att röra vid sidan av glaset. Kartong har inga av metallens egenskaper, så den kan ligga på glaset utan att påverka resultatet av experimentet. 


Genom att göra detta är anslutningen till batteriet klar och den elektriska strömmen från batteriet kan släppas ut i vattnet. 
För att detta experiment ska fungera bör pennornas grafit inte röra vid sidan av glaset. Så kontrollera det igen och flytta pennorna om det behövs. 
När du kopplar krokodilklämmorna till batteriet och grafiten börjar elektriciteten att röra på sig direkt. Fler bubblor kommer upp från vätgas eftersom varje vattenmolekyl innehåller dubbelt så mycket väte som syre.
Att göra väte och syre genom elektrolys
Processen genom vilken vatten (H2O) bryts ner till olika typer av atomer eller grundämnen (väte och syre) med hjälp av elektricitet kallas elektrolys. Detta experiment har betydande konsekvenser för tillämpningarna av dessa två gaser, där väte är en av de renaste energikällorna vi har tillgång till. Det kan låta komplicerat, men det är lättare än du tror om du har rätt resurser, kunskap och kompetens.
Steg
Del 1 av 2: Ställa upp experimentet

1. Fyll ett 350 ml glas med varmt vatten. Du behöver inte fylla glaset till brädden, så lämna lite utrymme. När vattnet är varmt leder det ström bättre. Detta experiment fungerar dock bra även med kallt vatten.
- Du kan använda kranvatten eller vatten på flaska. Det spelar ingen roll vad du väljer.
- Varmare vatten har en lägre viskositet och låter jonerna som leder elektricitet röra sig mer fritt.

2. Lös upp 1 matsked (20 gram) bordssalt i vattnet. Du behöver bara hälla saltet i vattnet och rör om vattnet lite för att se till att saltet löser sig. Du har nu en saltlösning.

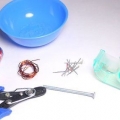
3. Vässa 2 HB-pennor i båda ändarna så att du kan se grafiten. Se till att ta bort radergummit i slutet av pennan. Du måste vässa pennorna tillräckligt långt så att grafiten är helt exponerad i båda ändarna.

4. Klipp ut en fyrkantig bit kartong som är tillräckligt stor för att täcka glaset. Använd kartong som är tillräckligt tjock och förblir stadig när du gör hål i den. Klipp till exempel en ruta ur en skokartong eller en annan kartong av tjock kartong.

5. Gör 2 hål i kartongbiten med de 2 pennorna. Använd själva pennorna för detta, eftersom de måste sitta stadigt i hålen så att de inte skiftar eller sjunker ner. Om grafiten träffar sidan eller botten av glaset kommer experimentet att avbrytas.
Del 2 av 2: Kör experimentet

1. Anslut ändarna på krokodilklämmorna till batteriets poler. Batteriet är där den elektriska kraften kommer ifrån och alligatorklämmorna ser till att den strömmen transporteras till vattnet. Fäst en krokodilklämma till den positiva polen och en krokodilklämma till den negativa polen.
- Använd ett 6-volts batteri för detta. Om du inte hittar det, använd ett 9-volts batteri.
- Du kan köpa den här typen av batteri i nästan varje stormarknad och varuhus.

2. Fäst de andra ändarna av alligatorklämmorna på pennorna. Se till att metalldelen av krokodilklämman vidrör pennans grafit. Du kan behöva skära lite trä från pennorna för att se till att alligatorklämmorna kommer i full kontakt med grafiten.

3. Lägg kartongbiten ovanpå glaset så att pennorna sänks under vatten. På grund av hur du precis klippt kartongen ska den nu sitta fint ovanpå glaset. Försök att göra detta noggrant så att pennorna som sticker genom pappen inte förskjuts eller glider.

4. Se hur vattnet sönderdelas till väte och syre. Bubblor bör nu stiga upp från grafitens nedsänkta punkter. Detta innebär att vätgasen och syrgasen delas. Vätgas bubblar upp från pennan som är ansluten till den negativa terminalen och syrgas upp från pennan som är ansluten till den positiva terminalen.
Tips
- Om du inte hittar pennor med grafitbly kan du också använda korta trådar. Linda ena änden runt batteriet och lägg den andra i vattnet. Detta har samma effekt som att använda pennor.
- Använd ett batteri med en annan spänning. Detta påverkar mängden elektrisk ström som passerar genom vattnet, vilket i sin tur påverkar hastigheten med vilken vattenmolekylerna delas.
Varningar
- Om du använder en elektrolyt som ett salt för att förbättra ledningsförmågan, var medveten om att en liten mängd klor produceras som en biprodukt. Detta räcker inte för att vara farligt, men du kan känna lukten av en lätt klorlukt.
- Utför detta experiment under uppsikt av vuxen eftersom du kommer att arbeta med elektricitet och gaser som, hur osannolikt de än är, kan vara skadliga för dig.
Förnödenheter
- 2 st HB pennor
- 1 6- eller 9-volts batteri
- Glas med en kapacitet på 350 ml
- 2 alligatorklämmor
- Pennvässare
- bordssalt
"Att göra väte och syre genom elektrolys"
Оцените, пожалуйста статью