Du kan ändra denna formel om du vill hitta förändringen i mängden värme, snarare än den specifika värmen. Ekvationen blir då: ΔQ = mCsidT 

m = 350 g Q = 34.700 joule ΔT = 173ºC - 22ºC = 151ºC Csid = okänt 
Den ursprungliga ekvationen: Csid = Q/mAT c = 34 700 J/(350 g x 151 ºC) 
Csid =34.700 J/(350g x 151ºC) Csid =34.700 J/(52850g x ºC) Csid = 0,65657521286 J/(g x ºC)
Beräkna specifik värme
Specifik värme är den mängd energi som krävs för att höja temperaturen på 1 gram av ett ämne med 1 grad Celsius. Den specifika värmen hos ett ämne beror både på molekylstrukturen och på vilken fas ämnet befinner sig i. Upptäckten av specifik värme gav impulser till studiet av termodynamik, studiet av energiomvandling genom värme och driften av system. Specifik värme och termodynamik används flitigt inom kemi, kärnkraftsforskning och aerodynamik, såväl som i vardagen i det centrala värme- och kylsystemet i din bil. Om du vill veta hur man beräknar specifik värme, ta följande steg.
Steg
Metod 1 av 2: Lär dig grunderna

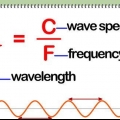
1. Bekanta dig med termerna som används för att beräkna specifik värme innan du lär dig om formlerna som ska användas. Lär dig känna igen de olika termerna och vad de betyder. Här är de termer som oftast används när man beräknar den specifika värmen för ett ämne: Massan representeras av "m". Mängden värme representeras av "F". Mängden värme representeras av "J", eller Joules. "t" är ämnets temperatur. Specifik värme representeras av "Csid".
- Delta, eller det "Δ" symbol, representerar förändringen av en variabel.
- Till exempel, om den första temperaturen (T1) är 150ºC och den andra (T2) 20ºC, då är ΔT, eller temperaturförändringen, lika med 150ºC - 20ºC eller 130ºC.

2. Ekvationen för specifik värme. När du väl är bekant med termerna som används för att beräkna specifik värme, bör du nu lära dig deras ekvation. Formeln är: Csid = Q/mAT.
Metod 2 av 2: Beräkna specifik värme

1. En närmare titt på jämförelsen. Vad som behövs för att beräkna specifik värme. Anta att du har följande problem: Beräkna den specifika värmen för 350 g av ett okänt ämne, om du har 34.Tillsätt 700 Joule värme, och temperaturen stiger från 22ºC till 173ºC, utan fasförändring.

2. Lista kända och okända faktorer. När problemets nyhet tar slut kan du börja skriva ner varje känd och okända variabel för att få en bättre uppfattning om vad du har att göra med. Här är vad du behöver göra:

3. Koppla in de kända faktorerna i ekvationen. Du vet värdet av allt annat än "Csidc", så du måste använda resten av faktorerna i ekvationen och lösa för "Csid". Så här fungerar det:

4. Lös ekvationen. Nu när du har använt alla kända faktorer i ekvationen är resten enkel matematik. Den specifika värmen är 0,65657521286 J/(g x ºC).
Tips
- SI (Systeme International) definierar specifik värme som Joule per grad Celsius per gram. Men antalet kalorier per grad Fahrenheit per pund används fortfarande i det kejserliga enhetssystemet.
- Metall värms upp snabbare än vatten eftersom den har låg specifik värme.
- En kalorimeter kan ibland användas under en kemisk reaktion, när värme transporteras.
- När man löser sådana problem är det viktigt att avbryta enheterna mot varandra, där så är möjligt.
- Den specifika värmen hos många föremål kan hittas i speciella uppslagsböcker eller online.
- Temperaturförändringen är större i material med låg specifik värme, förutsatt att alla andra förhållanden förblir oförändrade.
- Formeln för att beräkna matens specifika värme. Csid = 4.180 x b + 1.711 x p + 1.928×f+1.547 x c + 0.908 x a är ekvationen som används för att beräkna matens specifika värme. "W" är procentandelen vatten, "sid" är procentandelen protein, "f" är procentandelen fett, "c" är andelen kolhydrater och "a" är procentandelen kol. Denna ekvation tar hänsyn till massan (x) av alla fasta ämnen som utgör maten. Den specifika värmen uttrycks i kJ/(kg-K).
"Beräkna specifik värme"
Оцените, пожалуйста статью